Biogéochimie du plénum
Page 1 sur 1
 Biogéochimie du plénum
Biogéochimie du plénum
Bonjour à tous,
Suite à une demande du membre "Jean Robert" sur la chimie ou plutôt la biogéochimie du plénum, voici la réponse de Jean Jaubert que je tiens une fois de plus à remercier pour le temps qu'il consacre à nous répondre.
A mon avis le plénum n'est pas le siège d'une chimie (ou plutôt biogéochimie) particulière. C'est une simple voie de passage qui facilite la micro percolation du sédiment induite par le brassage. Certes, l'injection de CO2 pourrait faire baisser le pH de l'eau interstitielle - ce qui aurait pour effet d'accélérer la dissolution du carbonate de calcium et d'augmenter l'efficacité du RAC intégré que constitue la couche épaisse de sédiment - mais comment réguler cette injection pour éviter que du CO2 ne passe dans l'eau de l'aquarium et ne fasse baisser son pH?
Cela semble très risqué !
"En parcourant la littérature, j'en viens très doucement aux conclusions qui suivent:"
De quelle littérature s'agit-il ? Il faudrait que JR cite ses sources.
JR pourrait-il préciser ce qu'il entend par : "Il faut obligatoirement générer entre l'eau du plenum et l'eau libre de surface un potentiel redox." ?
Un potentiel redox (redox) se mesure en mV (valeurs positives ou négatives) par rapport à un potentiel de référence. A l'image de ce qui se passe dans la nature, le redox de l'eau de l'aquarium, qui circule à la surface du sédiment, est positif tandis que celui des couches hypoxiques du sédiment de même que (je suppose) celui du plénum est négatif.
Cet état des choses est la conséquence des processus biogéochimiques qui se produisent dans le sédiment ; notamment ceux qui sont responsables du recyclage de la matière organique détritique biodégradable.
Dans les couches superficielles, des microorganismes hétérotrophes minéralisent cette matière organique par oxydation en consommant l'oxygène de l'eau interstitielle. Ensuite, le NH4, issus de cette minéralisation, est oxydé en deux étapes (nitritation et nitratation) par des microorganismes autotrophes par chimiosynthèse. En respirant, les organismes (ciliés, vers, nématodes etc.) qui vivent à l'intérieur du sédiment consomment aussi de l'oxygène. De ce fait, l'eau qui circule lentement entre les grains de sable perd peu à peu de l'oxygène et un gradient de pO2 (concentration d'oxygène), décroissant en fonction de la profondeur, s'instaure automatiquement dans l'épaisseur d'une couche de sédiment. A une profondeur (éloignement de l'interface eau - sédiment) variable selon que la micro percolation est plus ou moins intense (cela dépend de la granulométrie et des forces d'advection dues à l'agitation), le sédiment devient hypoxique, puis anoxique. A ce stade, comme il n'y très peu (ou plus du tout) d'oxygène dans l'eau interstitielle, la matière organique résiduelle est oxydée par des bactéries hétérotrophes dénitrifiantes qui utilisent l'oxygène des ions nitrates (NO3-) qu'elles réduisent en azote moléculaire (N2).
La pO2 de l'eau d'un aquarium qui héberge de nombreux organismes photosynthétiques, varie considérablement au cours de la journée dès lors qu'il est modérément brassé (3-5 fois son volume par heure) et dépourvu de diffuseur d'air et (ou) d'écumeur. Pendant la période d'éclairement, la production d'oxygène par photosynthèse (essentiellement algues et coraux symbiotiques) est largement supérieure à la consommation (notamment celle des plantes, des coraux, des poissons etc. qui respirent continuellement). De ce fait, l'eau de l'aquarium est rapidement sursaturée en oxygène. Au niveau de l'interface eau - sédiment, la production d'oxygène des algues microscopiques attachées aux grains de sable fait que la pO2 de l'eau interstitielle est plus élevée que celle de l'eau de l'aquarium. Pendant la période d'obscurité, la photosynthèse s'arrête et la production d'oxygène cesse et la pO2 diminue alors de façon continue. En fin de nuit, l'eau est largement sous-saturée. A l'intérieur du sédiment, la pO2 de l'eau interstitielle varie au cours de la journée en fonction de la pO2 de l'eau de l'aquarium. L'année dernière, j'ai mesuré ces variations au niveau de l'interface sédiment - plénum (données non publiées) dans un aquarium contenant un sédiment grossier (sable de corail 2-5mm) et doté d'un brassage modéré (environ 3 fois le volume par heure). Ces mesures ont montré que l'eau interstitielle des couches profondes du sédiment (et donc aussi l'eau du plénum) n'était hypoxique que pendant la nuit lorsque que la p02 (pression partielle d'oxygène) de l'eau avait baissé aux environs de 50% de la saturation.
En, conséquence, dans un aquarium très brassé et (ou) longuement éclairé les couches profondes du sédiment ne sont pas suffisamment longtemps hypoxiques pour que la dénitrification et (ou) l'anammox (ou les deux) éliminent la totalité du NH4+ produit par l'excrétion des poissons et par la dégradation de la matière organique ainsi que tout le NO2- et le NO3- produits par les processus de nitrification. Dans ce cas, en limitant la sursaturation à quelques %, l'aération de l'eau (uniquement pendant la période d'éclairement par diffuseur d'air et/ou écumage) permettrait de remédier à cette situation en allongeant la durée de la période pendant laquelle les couches profondes du sédiment sont hypoxiques. Cependant, en cas de pollution organique accidentelle (par exemple organisme mort non retiré) les risques de poussée de NH4+, de NO2- et de H2S seraient beaucoup plus élevés que dans un aquarium dont l'eau est très sursaturée en oxygène.
"Le moteur de ce potentiel est du surtout à l'activité biochimique oxydante à la surface de l'eau et réductrice dans les couches profondes du sable et le plenum".
Oui, c'est aussi ce qui se passe partout dans la nature.
"Sans ce potentiel redox, la méthode jaubert ne fonctionne pas car la dénitrification "anaérobique "par consommation d'oxygène "va accumuler les sédiments dans le plenum et polluer le bac. Le sable joue donc un rôle membrane doublement perméable."
L'oxygène consommé par les bactéries hétérotrophes dénitrifiantes (et qu'elles utilisent pour oxyder le carbone organique dont elles se nourrissent) provient des ions nitrates (NO3-) qui sont réduits en azote moléculaire (N2). Autant que je sache, il n'y a aucun rapport entre l'activité de ces bactéries et l'accumulation de sable dans le plenum. Ce n'est pas l'activité des bactéries hétérotrophes dénitrifiantes, mais la bioturbation des organismes de l'endofaune qui peut faire passer, à travers la grille qui délimite le plénum, des particules fines inertes provenant du sédiment et (ou) des déjections des organismes qui le peuplent. Pour barrer le passage à ces particules fines inertes il suffit de couvrir la grille avec un voile géotextile.
"D'après certaines mesures ce potentiel est de l'ordre de 400mv/10cm soit un champ électrique de 4v/m. Il correspond grosso modo à une différence de pH entre l'eau oxygénée de surface et l'eau du plénum qui est plus acide vu sont état hypoxique."
De quelles mesures s'agit-il ? Dans quelles conditions on-t-elles été faites ? Il faudrait que JR cite sa (ou ses) source(s). Le pH ne dépend pas directement de la présence ou de l'absence d'oxygène, mais de celles de protons (H+) résultant de réactions telles que l'ionisation d'acides, la nitrification etc.
"Le sable, sa porosité et ses bactéries jouent donc un rôle de pile à combustible."
Certes, on peut transformer une couche de sédiment comportant des couches oxydées et hypoxiques (ou) anoxiques, en pile à combustible, mais à condition d'y introduire des électrodes.
De plus, je ne vois pas quelle manière la conversion du sédiment d'un aquarium en pile pourrait améliorer le son fonctionnement.
Depuis une vingtaine d'année des chercheurs ont étudié la possibilité de tirer de l'énergie électrique des processus biogéochimiques impliqués dans le recyclage de la matière organique détritique biodégradable qui s'accumule dans les sédiments marins. Les mécanismes, que ces travaux encore au stade expérimental exploitent, sont illustrés de façon très simplifiée par le schéma ci-dessous.
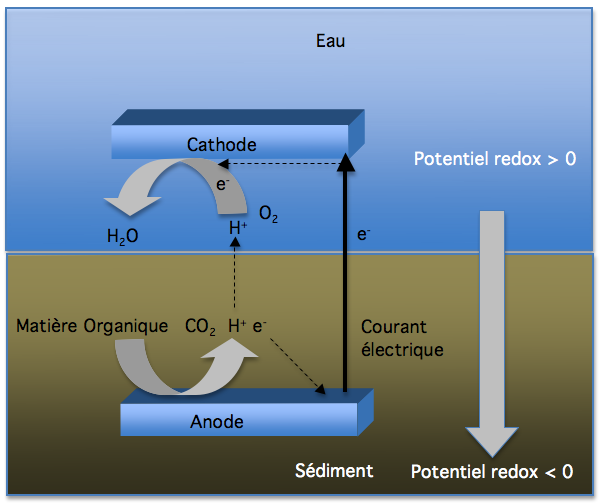
Les microorganismes responsables de ce recyclage jouent deux rôles clé. En premier lieu, ils établissent un gradient décroissant d'oxygène et de redox. En second lieu, ils libèrent de protons (H+) et des électrons (e-). Des électrons circulent entre les électrodes, générant un courant électrique, dès que celles-ci sont reliées par un fil conducteur isolé.
"En outre, certaines mesures de température montrent que l'eau du plenum est légèrement plus froide que l'eau libre de surface vu les réactions endothermiques (consommatrices de chaleur)."
De quelles mesures s'agit-il? Dans quelles conditions on-t-elles été faites? Mes propres mesures montrent qu'il y a, effectivement, une différence de quelques dixièmes de °C entre l'eau du plénum et celle de l'aquarium.
"En ce qui concerne le brassage, je pense que ce n'est pas le débit qui compte mais bien la force de l'ampleur instantanée en situation alternée (balancing) en vue de créer un "roulis" qui permet aux sédiments superficiels d'êtres fragmenter en petites particules et de progressivement s'introduire dans les interstices du sable et servir de combustible et de nutriment pour les bactéries ana ou hypoxique."
Le sédiment est une matière minérale (carbonate de calcium). Il ne peut donc pas servir de combustible pour les bactéries dénitrifiantes qui métabolisent de la matière organique. Par ailleurs, il est inutile de créer une circulation alternée pour booster la percolation. Des problèmes sont souvent provoqués par un excès de percolation provoqué par un excès de brassage. Les roches et les parois de l'aquarium sont des obstacles qui provoquent suffisamment de tourbillons pour assurer une percolation suffisante du sédiment.
"Là est aussi mon idée de vouloir introduire une pleine activité hypoxique dans le plenum à l'aide de pierres mortes et d'asphyxier l'eau du plenum avec une diffusion de co2 et peut être même dans certaines situations de le refroidir par un simple serpentin."
Une pierre morte n'aurait strictement aucune activité biologique consommatrice d'oxygène et ne pourrait donc absolument pas asphyxier l'eau du plénum.
Jean Jaubert
Suite à une demande du membre "Jean Robert" sur la chimie ou plutôt la biogéochimie du plénum, voici la réponse de Jean Jaubert que je tiens une fois de plus à remercier pour le temps qu'il consacre à nous répondre.
A mon avis le plénum n'est pas le siège d'une chimie (ou plutôt biogéochimie) particulière. C'est une simple voie de passage qui facilite la micro percolation du sédiment induite par le brassage. Certes, l'injection de CO2 pourrait faire baisser le pH de l'eau interstitielle - ce qui aurait pour effet d'accélérer la dissolution du carbonate de calcium et d'augmenter l'efficacité du RAC intégré que constitue la couche épaisse de sédiment - mais comment réguler cette injection pour éviter que du CO2 ne passe dans l'eau de l'aquarium et ne fasse baisser son pH?
Cela semble très risqué !
"En parcourant la littérature, j'en viens très doucement aux conclusions qui suivent:"
De quelle littérature s'agit-il ? Il faudrait que JR cite ses sources.
JR pourrait-il préciser ce qu'il entend par : "Il faut obligatoirement générer entre l'eau du plenum et l'eau libre de surface un potentiel redox." ?
Un potentiel redox (redox) se mesure en mV (valeurs positives ou négatives) par rapport à un potentiel de référence. A l'image de ce qui se passe dans la nature, le redox de l'eau de l'aquarium, qui circule à la surface du sédiment, est positif tandis que celui des couches hypoxiques du sédiment de même que (je suppose) celui du plénum est négatif.
Cet état des choses est la conséquence des processus biogéochimiques qui se produisent dans le sédiment ; notamment ceux qui sont responsables du recyclage de la matière organique détritique biodégradable.
Dans les couches superficielles, des microorganismes hétérotrophes minéralisent cette matière organique par oxydation en consommant l'oxygène de l'eau interstitielle. Ensuite, le NH4, issus de cette minéralisation, est oxydé en deux étapes (nitritation et nitratation) par des microorganismes autotrophes par chimiosynthèse. En respirant, les organismes (ciliés, vers, nématodes etc.) qui vivent à l'intérieur du sédiment consomment aussi de l'oxygène. De ce fait, l'eau qui circule lentement entre les grains de sable perd peu à peu de l'oxygène et un gradient de pO2 (concentration d'oxygène), décroissant en fonction de la profondeur, s'instaure automatiquement dans l'épaisseur d'une couche de sédiment. A une profondeur (éloignement de l'interface eau - sédiment) variable selon que la micro percolation est plus ou moins intense (cela dépend de la granulométrie et des forces d'advection dues à l'agitation), le sédiment devient hypoxique, puis anoxique. A ce stade, comme il n'y très peu (ou plus du tout) d'oxygène dans l'eau interstitielle, la matière organique résiduelle est oxydée par des bactéries hétérotrophes dénitrifiantes qui utilisent l'oxygène des ions nitrates (NO3-) qu'elles réduisent en azote moléculaire (N2).
La pO2 de l'eau d'un aquarium qui héberge de nombreux organismes photosynthétiques, varie considérablement au cours de la journée dès lors qu'il est modérément brassé (3-5 fois son volume par heure) et dépourvu de diffuseur d'air et (ou) d'écumeur. Pendant la période d'éclairement, la production d'oxygène par photosynthèse (essentiellement algues et coraux symbiotiques) est largement supérieure à la consommation (notamment celle des plantes, des coraux, des poissons etc. qui respirent continuellement). De ce fait, l'eau de l'aquarium est rapidement sursaturée en oxygène. Au niveau de l'interface eau - sédiment, la production d'oxygène des algues microscopiques attachées aux grains de sable fait que la pO2 de l'eau interstitielle est plus élevée que celle de l'eau de l'aquarium. Pendant la période d'obscurité, la photosynthèse s'arrête et la production d'oxygène cesse et la pO2 diminue alors de façon continue. En fin de nuit, l'eau est largement sous-saturée. A l'intérieur du sédiment, la pO2 de l'eau interstitielle varie au cours de la journée en fonction de la pO2 de l'eau de l'aquarium. L'année dernière, j'ai mesuré ces variations au niveau de l'interface sédiment - plénum (données non publiées) dans un aquarium contenant un sédiment grossier (sable de corail 2-5mm) et doté d'un brassage modéré (environ 3 fois le volume par heure). Ces mesures ont montré que l'eau interstitielle des couches profondes du sédiment (et donc aussi l'eau du plénum) n'était hypoxique que pendant la nuit lorsque que la p02 (pression partielle d'oxygène) de l'eau avait baissé aux environs de 50% de la saturation.
En, conséquence, dans un aquarium très brassé et (ou) longuement éclairé les couches profondes du sédiment ne sont pas suffisamment longtemps hypoxiques pour que la dénitrification et (ou) l'anammox (ou les deux) éliminent la totalité du NH4+ produit par l'excrétion des poissons et par la dégradation de la matière organique ainsi que tout le NO2- et le NO3- produits par les processus de nitrification. Dans ce cas, en limitant la sursaturation à quelques %, l'aération de l'eau (uniquement pendant la période d'éclairement par diffuseur d'air et/ou écumage) permettrait de remédier à cette situation en allongeant la durée de la période pendant laquelle les couches profondes du sédiment sont hypoxiques. Cependant, en cas de pollution organique accidentelle (par exemple organisme mort non retiré) les risques de poussée de NH4+, de NO2- et de H2S seraient beaucoup plus élevés que dans un aquarium dont l'eau est très sursaturée en oxygène.
"Le moteur de ce potentiel est du surtout à l'activité biochimique oxydante à la surface de l'eau et réductrice dans les couches profondes du sable et le plenum".
Oui, c'est aussi ce qui se passe partout dans la nature.
"Sans ce potentiel redox, la méthode jaubert ne fonctionne pas car la dénitrification "anaérobique "par consommation d'oxygène "va accumuler les sédiments dans le plenum et polluer le bac. Le sable joue donc un rôle membrane doublement perméable."
L'oxygène consommé par les bactéries hétérotrophes dénitrifiantes (et qu'elles utilisent pour oxyder le carbone organique dont elles se nourrissent) provient des ions nitrates (NO3-) qui sont réduits en azote moléculaire (N2). Autant que je sache, il n'y a aucun rapport entre l'activité de ces bactéries et l'accumulation de sable dans le plenum. Ce n'est pas l'activité des bactéries hétérotrophes dénitrifiantes, mais la bioturbation des organismes de l'endofaune qui peut faire passer, à travers la grille qui délimite le plénum, des particules fines inertes provenant du sédiment et (ou) des déjections des organismes qui le peuplent. Pour barrer le passage à ces particules fines inertes il suffit de couvrir la grille avec un voile géotextile.
"D'après certaines mesures ce potentiel est de l'ordre de 400mv/10cm soit un champ électrique de 4v/m. Il correspond grosso modo à une différence de pH entre l'eau oxygénée de surface et l'eau du plénum qui est plus acide vu sont état hypoxique."
De quelles mesures s'agit-il ? Dans quelles conditions on-t-elles été faites ? Il faudrait que JR cite sa (ou ses) source(s). Le pH ne dépend pas directement de la présence ou de l'absence d'oxygène, mais de celles de protons (H+) résultant de réactions telles que l'ionisation d'acides, la nitrification etc.
"Le sable, sa porosité et ses bactéries jouent donc un rôle de pile à combustible."
Certes, on peut transformer une couche de sédiment comportant des couches oxydées et hypoxiques (ou) anoxiques, en pile à combustible, mais à condition d'y introduire des électrodes.
De plus, je ne vois pas quelle manière la conversion du sédiment d'un aquarium en pile pourrait améliorer le son fonctionnement.
Depuis une vingtaine d'année des chercheurs ont étudié la possibilité de tirer de l'énergie électrique des processus biogéochimiques impliqués dans le recyclage de la matière organique détritique biodégradable qui s'accumule dans les sédiments marins. Les mécanismes, que ces travaux encore au stade expérimental exploitent, sont illustrés de façon très simplifiée par le schéma ci-dessous.

Les microorganismes responsables de ce recyclage jouent deux rôles clé. En premier lieu, ils établissent un gradient décroissant d'oxygène et de redox. En second lieu, ils libèrent de protons (H+) et des électrons (e-). Des électrons circulent entre les électrodes, générant un courant électrique, dès que celles-ci sont reliées par un fil conducteur isolé.
"En outre, certaines mesures de température montrent que l'eau du plenum est légèrement plus froide que l'eau libre de surface vu les réactions endothermiques (consommatrices de chaleur)."
De quelles mesures s'agit-il? Dans quelles conditions on-t-elles été faites? Mes propres mesures montrent qu'il y a, effectivement, une différence de quelques dixièmes de °C entre l'eau du plénum et celle de l'aquarium.
"En ce qui concerne le brassage, je pense que ce n'est pas le débit qui compte mais bien la force de l'ampleur instantanée en situation alternée (balancing) en vue de créer un "roulis" qui permet aux sédiments superficiels d'êtres fragmenter en petites particules et de progressivement s'introduire dans les interstices du sable et servir de combustible et de nutriment pour les bactéries ana ou hypoxique."
Le sédiment est une matière minérale (carbonate de calcium). Il ne peut donc pas servir de combustible pour les bactéries dénitrifiantes qui métabolisent de la matière organique. Par ailleurs, il est inutile de créer une circulation alternée pour booster la percolation. Des problèmes sont souvent provoqués par un excès de percolation provoqué par un excès de brassage. Les roches et les parois de l'aquarium sont des obstacles qui provoquent suffisamment de tourbillons pour assurer une percolation suffisante du sédiment.
"Là est aussi mon idée de vouloir introduire une pleine activité hypoxique dans le plenum à l'aide de pierres mortes et d'asphyxier l'eau du plenum avec une diffusion de co2 et peut être même dans certaines situations de le refroidir par un simple serpentin."
Une pierre morte n'aurait strictement aucune activité biologique consommatrice d'oxygène et ne pourrait donc absolument pas asphyxier l'eau du plénum.
Jean Jaubert

Joé- Admin
- Messages : 6906
Date d'inscription : 17/09/2011
Age : 58
Localisation : France
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum|
|
|


